近日,我院心脏大血管外科主动脉微创治疗团队在四川大学华西医院临床新技术项目(医临新-2018-091和20HXJS015)的支撑下,为一名69岁男性实施了“体外开窗自制内嵌式三分支支架全腔内修复A型主动脉夹层近端修复后再发主动脉弓部巨大动脉瘤手术”,术后4天患者顺利出院,经文献检索,目前国内尚未见相似手术病例报道。 患者吴先生,5年前因Stanford A型主动脉夹层于我院行“升主动脉及右半弓置换术”,此次因“胸痛1天”于我院就诊。增强CT示:A型主动脉夹层近端修复术后,主动脉弓部巨大动脉瘤形成,最大直径达58.1mm(图1)。患者主动脉弓部病变亟需解决,否则远期发生主动脉夹层甚至自发性破裂的风险较高,但再次开胸血管置换手术的巨大创伤和手术风险让患者及家属望而生畏,一度试图放弃手术治疗。华西医院心脏大血管外科主动脉微创治疗团队胡佳副教授向患者及家属耐心解释了疾病的特殊性和全腔内微创修复的可能性以及手术相关风险后,患者及家属果断选择了腔内修复手术拆除体内这一“定时炸弹”。 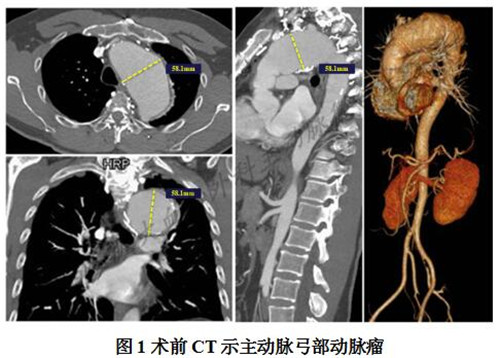
升主动脉置换术后再发主动脉弓部动脉瘤发病率约0.46%~0.5%。对于涉及主动脉弓部的主动脉夹层/动脉瘤,开放直视下行“全主动脉弓置换+降主动脉象鼻支架植入术”仍为临床首选治疗方案。随着腔内修复技术的发展,主动脉腔内修复结合分支动脉平行支架技术、体外预开窗或原位开窗技术为该类患者提供了新的选择。 对于本例患者而言,首次开胸手术后术野的广泛粘连和术中深低温停循环使得开放直视手术创伤及风险极高,患者及家属拒绝开放手术治疗。而常规的平行支架、体外预开窗或原位开窗等分支重建技术存在较高内漏风险,对于主动脉瘤患者而言,一旦发生内漏则功亏一篑。为了最大限度降低患者围术期风险,尽可能充分隔绝主动脉弓部动脉瘤,经过反复评估患者病情和主动脉条件,全科讨论手术方案后,团队决定为患者实施“自制内嵌式三分支支架全腔内修复术”。 第一步 体外测量+体外开窗+内嵌分支缝合
由于患者既往行升主动脉及右半弓置换手术,升主动脉人工血管为全腔内修复提供了可靠的近端锚定区,这也是实施本手术方案的先决条件。根据术前CTA详细测量的锚定距离和各分支开口的距离、直径以及相对弓顶的角度,并详细对比造影所测量的数据,确定预开窗位置(图2)。 
采用灼烧笔进行体外三开窗,截取合适直径和长度的分支动脉支架作为内嵌分支,分别缝合与窗口并缝制弹簧圈作为术中标记(图3)。再将自制内嵌式三分支支架回装到输送鞘内(图4)。 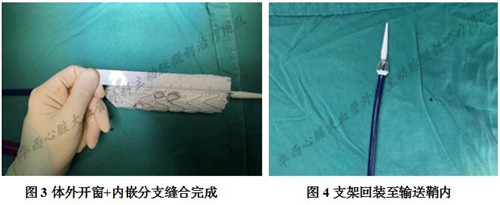
第二步 释放主动脉支架
全麻后暴露双侧颈动脉备用。穿刺右侧股动脉,左侧肱动脉植入5F导鞘备用。经右侧股动脉入路髂总—腹主—升主动脉上行并造影(图5),评估弓部病变和主要分支供血情况并核实术前CT测量数据。标记升主动脉人工血管位置,控制性降压。 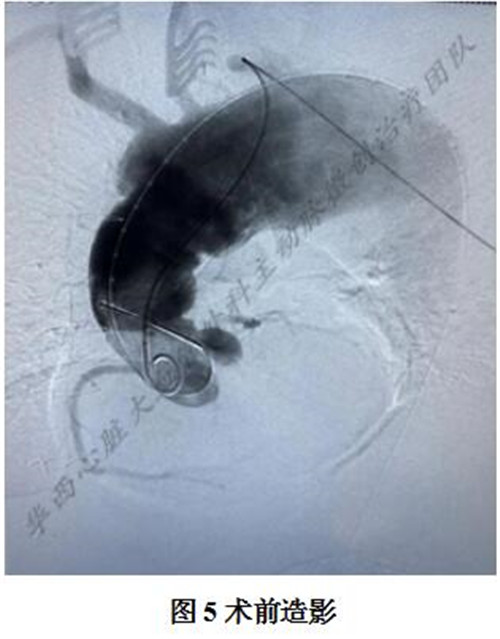
超硬导丝建立轨道后导入远端限制性支架,定位于胸降主动脉下段释放(图6),交换导入自制内嵌式三分支支架作为近端主体支架,将支架预先缝制的弹簧圈标记点分别对准无名动脉、左颈总动脉及左锁骨下动脉开口,支架近端定位于升主动脉人工血管内释放(图7)。 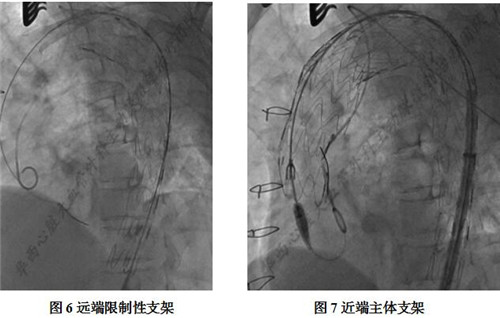
第三步 逐一释放弓上分支动脉支架
经右颈总动脉10F鞘引入导管导丝,配合选进无名动脉的内嵌分支中,造影确认后,导入无名动脉支架,近端定位完整重叠于内嵌分支的长度,释放支架,完成无名动脉重建。(图8) 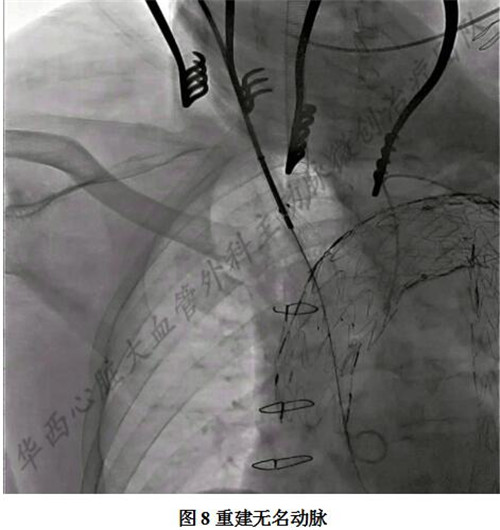
同上述方法重建左颈总动脉(图9)和左锁骨下动脉(图10) 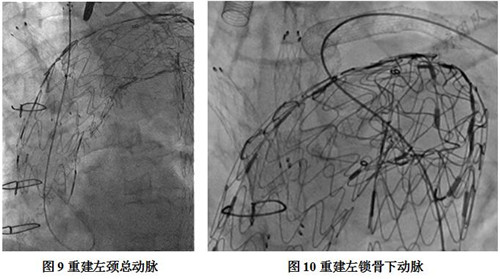 术后造影显示:主体支架定位准确;瘤体隔绝良好,无内漏;弓部三分支血流通畅;远段口径限制适度支架过度自然(图11)。整体效果满意,手术顺利结束(图12)。 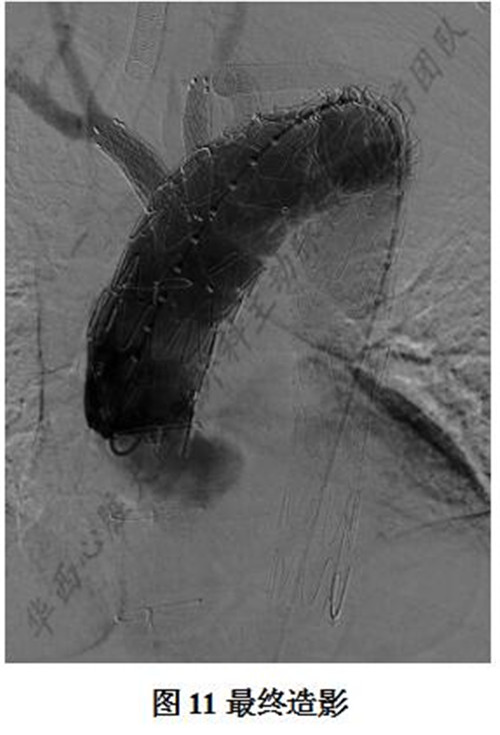
第四步 严密的术后监护+术后康复出院
手术结束后,患者转至胸心血管重症监护室。在重症监护室曹舸副主任医师以及曾玲护士长带领的医护团队的共同努力和细心照料下,患者术后6小时顺利拔除气管插管,第二天转回普通病房。术后复查夹层动脉瘤CTA显示主动脉弓部整体形态良好,弓上分支动脉血流通畅,动脉瘤完全隔绝,未见明显内漏(图13)。患者术后恢复顺利,无手术并发症发生,于术后第4天顺利出院。术后一月复查显示支架通畅,形态良好,无内漏(图14)。 
主动脉弓部病变是一类严重影响患者远期寿命的心血管疾病。传统正中开胸手术风险高,尤其是再次开胸手术。全腔内修复手术能够尽可能微创化隔绝病变部位,但应根据患者主动脉条件和病变特点,制定个体化的、精准化的腔内修复方案。本例体外开窗自制内嵌式三分支支架全腔内修复主动脉弓部动脉瘤手术的成功,展现出华西医院作为西南地区疑难重症中心的实力,诊疗过程中心脏大血管外科,麻醉科,胸心血管ICU等多学科团队的团结合作也为此类疑难重症患者保驾护航添加了一份强有力的保障。我们有能力,也有信心更加安全、微创和精准地祛除患者病痛,造福更多患者。
|


